Therapie der Multiple Sklerose
Vielfältiger Ansatz
Entscheidende Fortschritte sind in den vergangenen Jahren in der Behandlung der Multiplen Sklerose gemacht worden. Dabei kommt der schulmedizinischen Behandlung, der so genannten evidenzbasierten Medizin, die entscheidende Bedeutung zu. Evidenzbasiert bedeutet, dass es für die Behandlung eine wissenschaftlich nachgewiesene Wirksamkeit gibt. Besonders zu Beginn der Erkrankung, wenn die entzündliche Aktivität am stärksten ist, können die heute verfügbaren Medikamente ihre Wirkung entfalten. So früh und so konsequent wie möglich zu therapieren ist deshalb der entscheidende Ansatz für die moderne MS-Therapie.
Die Multiple Sklerose ist zum heutigen Zeitpunkt dennoch nicht heilbar. Vor Wunderheilungen muss man warnen. Solche – oft besonderes plakativ in der Laienpresse angepriesenen – Maßnahmen haben nichts mit der tatsächlich notwendigen ganzheitlichen Betrachtung und Behandlung zu tun. Der Erhalt der Lebensqualität des Betroffenen als auch dessen Psyche müssen im Auge behalten werden, da diese Faktoren einen positiven Einfluss auf den Verlauf der Krankheit ausüben können.
Möglichst früh und konsequent – die medikamentöse Therapie
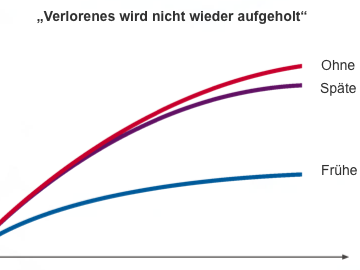 Verlorenes wird nicht wieder aufgeholt. Wer zu spät mit einer wirksamen Behandlung beginnt, wer abwartet, bis die Krankheit weiter fortgeschritten ist, bis Schübe häufiger werden oder der Behinderungsgrad höher wird, muss damit rechnen, dass er eine wichtige Chance zur Behandlung vertan hat. Die sofortige Behandlung schon beim ersten Auftreten von Krankheitszeichen, beim so genannten klinisch isolierten Syndrom (CIS), kann den Krankheitsverlauf um Jahre verzögern.
Verlorenes wird nicht wieder aufgeholt. Wer zu spät mit einer wirksamen Behandlung beginnt, wer abwartet, bis die Krankheit weiter fortgeschritten ist, bis Schübe häufiger werden oder der Behinderungsgrad höher wird, muss damit rechnen, dass er eine wichtige Chance zur Behandlung vertan hat. Die sofortige Behandlung schon beim ersten Auftreten von Krankheitszeichen, beim so genannten klinisch isolierten Syndrom (CIS), kann den Krankheitsverlauf um Jahre verzögern.
Es betrifft die Zeit, die vergeht, bis man nach dem ersten Symptom dann von einer klinisch gesicherten MS spricht. Dies gilt auch für die Zunahme des Behinderungsgrades und die Verhinderung von Schüben.
Mit dem Einsatz moderner Medikamente kann dieser Zeitraum um viele Jahre hinausgezögert werden. Je später die Behandlung beginnt, umso weniger effektiv ist diese.
Die Effektivität der Therapie sinkt mit der Dauer des Krankheitsverlaufes.
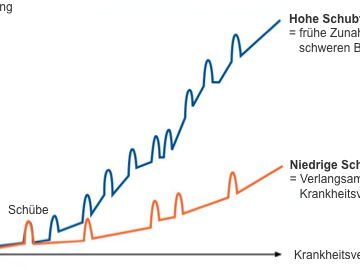
Die Schübe sind nur die Spitze des Krankheits-Eisberges. Die Multiple Sklerose schläft nie und läuft auch ohne spürbare Symptome und schubförmige Verschlechterungen ab. Es kommt zu weiteren Entzündungsschüben im Gehirn, die nur kernspintomographisch in aktiven kontrastmittelaufnehmenden Herden nachgewiesen werden können.
Einsatz der Medikamente – ein stufenweises Vorgehen
Wenn man die Multiple Sklerose – Behandlung einteilen möchte, so umfasst die Therapie, insbesondere die mit Medikamenten, unterschiedlicher Ziele. Bei Auftreten eines akuten Schubes muss rasch und konsequent behandelt werden (Schubtherapie).
Gleichzeitig sollte das Auftreten weiterer Schübe überhaupt verhindert und die Krankheit in ihrem Fortschreiten aufgehalten werden (Basistherapie). Verliert die Basistherapie an Wirksamkeit oder handelt es sich um eine hoch aktive MS, muss die Behandlung gegebenenfalls intensiviert werden (Eskalationstherapie). Entwickeln sich, trotz aller Bemühungen, deutliche Beeinträchtigungen verschiedener Körperfunktionen, wie z. B. Lähmungen oder Blasenstörungen, dann müssen diese ebenfalls behandelt werden (symptomatische Therapie). Ziel ist es dabei, zumindest die Lebensqualität der betroffenen Patienten zu verbessern.
Die sogenannte Basistherapie hat das Ziel, langfristig den Verlauf der Erkrankung positiv zu beeinflussen. Schübe sollen dann seltener auftreten und vor allem auch das Fortschreiten der Erkrankung soll eingeschränkt werden. In der Akutbehandlung steht in erster Linie der Krankheitsschub im Zentrum des Interesses; in der symptomatischen Therapie werden Begleiterkrankungen – Spastik, Blasenstörung, Müdigkeitssyndrom (Fatigue), die Uthoff-Symptomatik oder auch kognitive Störungen – behandelt. Unterstützende Maßnahmen zielen z. B. auf die Versorgung mit Hilfsmitteln. Hier sind auch krankengymnastische, physikalische und ergotherapeutische Behandlungsansätze anzuführen.
Eventuell können zur Krankheitsverarbeitung oder bei Konflikten psychotherapeutische und psychiatrische/psychopharmakologische Behandlungsverfahren angewandt werden.
 Die Multiple Sklerose Therapie Konsensusgruppe (MSTKG) hat eine Stufentherapie zur medikamentösen Behandlung der Multiplen Sklerose erarbeitet. Aktuell wird ergänzend auch im Krankheitsbezogenen KompetenzNetz MS (KKNMS) an der Standardisierung des therapeutischen Vorgehens gearbeitet. In der Schubtherapie wird derzeit der Einsatz von Cortison, Blutwäsche (Plasmapherese) oder Immunadsorption (Entfernung bestimmter Antikörper aus dem Blut) empfohlen. In der Basistherapie sollten aktuell Interferone, Glatirameracetat, Azathioprin und ab 2014 Dimethylfumarat und Teriflunomid eingesetzt werden. Weiter ist es möglich, Medikamente ohne spezifische Zulassung (Off Label) z. B. während einer bestehenden Schwangerschaft (Immunglobuline) oder bei Medikamentenunverträglichkeit anzuwenden (Methotrexat).
Die Multiple Sklerose Therapie Konsensusgruppe (MSTKG) hat eine Stufentherapie zur medikamentösen Behandlung der Multiplen Sklerose erarbeitet. Aktuell wird ergänzend auch im Krankheitsbezogenen KompetenzNetz MS (KKNMS) an der Standardisierung des therapeutischen Vorgehens gearbeitet. In der Schubtherapie wird derzeit der Einsatz von Cortison, Blutwäsche (Plasmapherese) oder Immunadsorption (Entfernung bestimmter Antikörper aus dem Blut) empfohlen. In der Basistherapie sollten aktuell Interferone, Glatirameracetat, Azathioprin und ab 2014 Dimethylfumarat und Teriflunomid eingesetzt werden. Weiter ist es möglich, Medikamente ohne spezifische Zulassung (Off Label) z. B. während einer bestehenden Schwangerschaft (Immunglobuline) oder bei Medikamentenunverträglichkeit anzuwenden (Methotrexat).
Ist die Wirksamkeit der Basistherapie erschöpft oder handelt es sich um eine hoch aktive MS, wird als Eskalationstherapie, der Einsatz von Fingolimod, Natalizumab, Mitoxantron oder seit 2013 Alemtuzumab erwogen. Als weitere Stufe kann auch an den Einsatz von Cyclophosphamid – bis hin zur Immunablation (vollständige Unterdrückung des Immunsystems und Stammzellentransplantation) – gedacht werden.
Konsequent durchführen – die Basistherapie
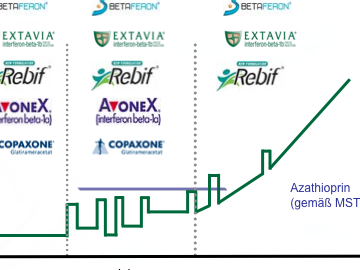 An Interferonen stehen derzeitig Betaferon®, Extavia®, Avonex® und Rebif® zur Verfügung, der Wirkstoff Glatirameracetat ist unter dem Handelsnamen Copaxone® erhältlich. Das Anwendungsfeld (Indikationsspektrum) der einzelnen Wirksubstanzen ist unterschiedlich. Interferon beta 1b ist für das klinisch isolierte Syndrom (CIS), über die schubförmige Multiple Sklerose bis zur sekundär chronisch progredienten Verlaufsform der Erkrankung zugelassen. Glatirameracetat, Interferon beta 1a in der intramuskulären Applikationsform und in der subkutanen Applikation ist im CIS-Stadium und bei der schubförmigen MS-Behandlung zugelassen.
An Interferonen stehen derzeitig Betaferon®, Extavia®, Avonex® und Rebif® zur Verfügung, der Wirkstoff Glatirameracetat ist unter dem Handelsnamen Copaxone® erhältlich. Das Anwendungsfeld (Indikationsspektrum) der einzelnen Wirksubstanzen ist unterschiedlich. Interferon beta 1b ist für das klinisch isolierte Syndrom (CIS), über die schubförmige Multiple Sklerose bis zur sekundär chronisch progredienten Verlaufsform der Erkrankung zugelassen. Glatirameracetat, Interferon beta 1a in der intramuskulären Applikationsform und in der subkutanen Applikation ist im CIS-Stadium und bei der schubförmigen MS-Behandlung zugelassen.
Man unterscheidet zwei verschiedene Arten von Interferon: Interferon beta 1a und Interferon beta 1b. Interferon beta 1a ist dem natürlichen, menschlichen Interferon beta ähnlicher; es wird aus Zellen von Hamstereierstöcken gewonnen. Interferon beta 1b wird biotechnologisch aus Bakterien (E. Coli) hergestellt.
Die Interferone sind Medikamente, welche die fehlgeleiteten Aktivitäten des körpereigenen Immunsystems verändern. Interferone verringern einerseits die Aktivierung und Vermehrung von Entzündungszellen und reduzieren auch die Produktion von entzündungsfördernden Botenstoffen im Gehirn. Schließlich sind Interferone offenbar in der Lage, die Produktion entzündungshemmender Botenstoffe zu fördern. Weitergehend verringern sie die Durchlässigkeit der Blut-Hirn-Schranke für fehlgesteuerte Immunzellen. Zu Glatirameracetat ist festzuhalten, dass es wohl zu einem Wechsel von schädigend (toxisch) zu schützend (protektiv) wirkenden T-Zellen kommt; dies gewissermaßen über eine Impfung mit der Substanz Glatirameracetat. Es wird auch angenommen, dass Glatirameracetat Faktoren anregt, die einen Nervenzellschutz bewirken können.
Dimethylfumarsäure (Handelsname Tecfidera®) wirkt über zellschützende Mechanismen, Teriflunomid (Handelsname Aubagio®) hemmt die Vermehrung krankheitsrelevanter (autoreaktiver) Immunzellen. Dimethylfumarsäure wird zweimal am Tag als Tablette eingenommen, Teriflunomid ist ebenfalls eine oral einzunehmendes Medikament; hier reicht eine Tablette am Tag zur Behandlung aus.
Dimethylfumarsäure (Fumarsäure) ist eine (zweimal täglich als Tablette einzunehmende) Substanz, die sich in der Behandlung der Schuppenflechte über viele Jahre bewährt hat. Zwischenzeitlich ist in Studien auch deren Wirksamkeit bei der Multiplen Sklerose festgestellt worden. Durch eine Veränderung der molekularen Struktur dieser Substanz konnte im Vergleich zur bisherigen Anwendung in der Dermatologie eine bessere Verträglichkeit des Medikamentes erreicht werden. Es wirkt über komplexe neuroprotektive Mechanismen (Fumarsäure spielt eine Schlüsselrolle in der oxidativen Energiegewinnung über den Zitratzyklus) im Immunsystem und auch im ZNS. Neben einer guten Wirkung auf die Schubratenreduktion (40 bis 50 %) und auch auf die im Kernspin nachweisbaren Krankheitsaktivität, ist die Dimethylfumarsäure geeignet, die Krankheitsprogression (ca. 3 8%) zu lindern.
Teriflunomid wird einmal täglich eingenommen. Es ist eine Substanz, die aufgrund eines besonderen Mechanismus immer wieder aus dem Darm wiederaufgenommen wird und deshalb sehr lange im Körper verbleibt. Man nimmt eine Tablette pro Tag und erreicht damit wirksame Spiegel. Die Substanz hemmt die Bildung autoreaktiver (für die Entzündung der MS) bedeutsamer Immunzellen, ohne wesentlich die allgemeine Infektabwehr zu beeinträchtigen. Wie auch die anderen Basistherapeutika wirkt die Substanz gut auf die Schubaktivität und insbesondere auch auf die Krankheitsprogression (ca. 30 %). Eine gute Wirksamkeit ist auch im Blick auf die Kernspinaktivität nachgewiesen.
Inzwischen neu zugelassen ist auch Alemtuzumab für aktive Formen der MS. Diese Therapie ist richtigerweise nicht als Eskalationsmaßnahme verfügbar – dennoch soll sie aufgrund der Besonderheiten in der Anwendung und in der Überwachung nach den Behandlungszyklen weiter unten besprochen werden.
Sogenannte Immunsuppressiva (Azathioprin) hemmen das Wachstum von Immunzellen und damit die Bildung von Antikörpern gegen die Markscheiden. Azathioprin wird als Tablette täglich gegebenenfalls mehrfach verabreicht.
Grundsätzlich ist eine langfristige Behandlung durch die Basismedikation notwendig. Ein kurzfristiger Effekt darf nicht erwartet werden.
Alles was wirkt hat Begleiterscheinungen – die Nebenwirkungen
Die häufigsten Nebenwirkungen der Interferone sind grippeähnliche Symptome, insbesondere zu Beginn der Therapie. Ebenso treten häufig Hautreaktionen an der Einstichstelle auf. Interferone müssen im Fall von Betaferon®, Extavia® und Rebif® unter die Haut (subkutan) gegeben werden, Avonex® hingegen wird in den Muskel gespritzt (intramuskulär). Die grippeähnlichen Symptome treten bei bis zu 70 % aller Patienten zu Beginn auf, gelegentlich von Gliederschmerzen begleitet. Kältegefühl, Abgeschlagenheitsgefühl, auch Kopfschmerzen, sind denkbar. Diese Nebenwirkungen dauern in der Regel nicht länger an und können zudem durch Schmerzmedikamente, wie z. B. Ibuprofen, Paracetamol oder Novaminsulfon gelindert werden. In der Regel lassen die Nebenwirkungen der Interferone in den ersten Monaten nach oder verschwinden ganz (nur in seltenen Fällen halten die Nebenwirkungen länger an). Teilweise kann man auch durch einen Wechsel des Medikamentes die Nebenwirkungen lindern.
Die Substanzen können in der Schwangerschaft und Stillzeit nicht angewendet werden. Häufig findet man als Nebenwirkung der Behandlung eine vorübergehende Leberwerterhöhung; insbesondere zu Beginn der Therapie. Es können gelegentlich auch allergische Reaktionen, ein Abfall von weißen Blutkörperchen oder ein Blutplättchenmangel beobachtet werden. Es wird immer wieder auch auf die Bildung von Antikörpern hingewiesen, welche die Wirkung der Interferone zumindest teilweise aufheben können. Weiter wird zu Beginn einer Interferon-Behandlung eine Verstärkung von Lähmungserscheinungen (spastische Paresen), besonders an den unteren Gliedmaßen, beobachtet.
Grundsätzlich ist es wichtig, sich in der Anwendung der Substanzen gut schulen zu lassen. Die hygienischen Bedingungen müssen dabei eingehalten werden, um keine Infektion der Injektionsstellen zu riskieren.
Tipp: Die Injektionslösung sollte körperwarm injiziert werden, nach der Injektion ist eine vorsichtige und sanfte Massage der Injektionsstelle hilfreich.
Die Haut ist vor und nach der Injektion zu kühlen. Wird die Injektion am späten Abend gegeben, können die Nebenwirkungen gewissermaßen verschlafen werden. Durch fieber- und schmerzlindernde Medikamente (siehe oben) kann ebenfalls grippeähnlichen Nebenwirkungen vorgebeugt werden. Diese sollten, vornehmlich zu Beginn der Behandlung, einige Stunden vor und nach der Injektion eingenommen werden.
Glatirameracetat wird wie die subcutan zu applizierenden Interferone täglich unter die Haut gespritzt.
Wie bei den Interferonen gilt, dass Glatirameracetat in der Schwangerschaft und Stillzeit nicht eingesetzt werden darf. Unwohlsein, beschleunigter Herzschlag, Schmerzen im Bereich der Brust, Atemnot, Rötung im Gesicht oder am Körper können neben einer allergischen Reaktion bei einer entsprechenden Behandlung auftreten. Diese Begleiterscheinungen sind eher selten und treten in der Regel nur zu Beginn der Behandlung auf. Gelegentlich kommt es bei längerer Anwendung zu Hautveränderungen im Unterhautfettgewebe, die dann als Einziehungen äußerlich erkennbar sind.
Die seit 2013 neu verfügbaren Medikamente haben ein anderes Nebenwirkungsspektrum.
Bei Teriflunomid sind in den ersten sechs Monaten eine (sich rückbildende) Haarausdünnung neben potentiellen Leberwerterhöhungen zu bedenken; eine sichere Empfängnisverhütung ist geboten. In ganz seltenen Fällen sind auch Neuropathien beschrieben worden.
Bei Dimethylfumarsäure sind in den ersten Monaten Übelkeit, Magen-Darm-Probleme und (schon im Einsatz von Glatirameracetat bekannt) Flush anzuführen.
Im akuten Fall – die Schubtherapie
 Ziel der Schubtherapie ist es, die Schubdauer zu verkürzen, die Entzündungsaktivität zu vermindern und die Symptome relativ rasch zur Rückbildung zu bringen. In der Schubtherapie hat sich der Einsatz von Cortison bewährt. Schübe sollen grundsätzlich verhindert werden, da weniger Schübe auch einen günstigeren Verlauf der Erkrankung bedeuten können. Ein akuter Schub muss daher rasch, konsequent und unverzüglich behandelt werden. Dies kann entweder durch eine Einspritzung direkt in die Vene (intravenös), über Tabletten (oral) oder auch durch eine intrathekale Injektion von Cortison geschehen. Intrathekal bedeutet, dass das Cortison in der Nähe des Rückenmarks verabreicht wird (d.h. in das Nervenwasser appliziert wird), damit das Medikament möglichst nahe am Ort des Geschehens wirksam werden kann.
Ziel der Schubtherapie ist es, die Schubdauer zu verkürzen, die Entzündungsaktivität zu vermindern und die Symptome relativ rasch zur Rückbildung zu bringen. In der Schubtherapie hat sich der Einsatz von Cortison bewährt. Schübe sollen grundsätzlich verhindert werden, da weniger Schübe auch einen günstigeren Verlauf der Erkrankung bedeuten können. Ein akuter Schub muss daher rasch, konsequent und unverzüglich behandelt werden. Dies kann entweder durch eine Einspritzung direkt in die Vene (intravenös), über Tabletten (oral) oder auch durch eine intrathekale Injektion von Cortison geschehen. Intrathekal bedeutet, dass das Cortison in der Nähe des Rückenmarks verabreicht wird (d.h. in das Nervenwasser appliziert wird), damit das Medikament möglichst nahe am Ort des Geschehens wirksam werden kann.
In der Regel wird über drei bis fünf Tage 1000 mg Methylprednisolon intravenös gegeben.
Bleibt ein Behandlungserfolg aus bzw. ist die Rückbildung der Symptome deutlich verzögert, kann diese Therapie nach 14 Tagen wiederholt werden. Sollte die Therapie weiterhin keine befriedigende Wirkung zeigen, ist eine Plasmapherese (Blutwäsche) oder eine Immunadsorption (spezifische Blutwäsche) möglich.
Neben der Pulstherapie wird immer wieder auch eine so genannte Cortisonkur angewandt. Hier wird über 3 bis 5 Tage hochdosiert Cortison gegeben – wie bei der Pulstherapie – danach wird über 1 bis 2 Wochen die Dosis langsam herabgesetzt. Bei Herden im Bereich des Rückenmarks, vornehmlich auf der Höhe des Brustmarks und auch der Lenden (Conus medullaris), kann ein Cortison-Präparat (40 mg Triamcinolonacetonid Kristallsuspension) in die Nähe des Rückenmarks (intrathekal) injiziert werden. Spastische Paraparesen und Schübe, die in erster Linie den Gebrauch der unteren Gliedmaßen beeinträchtigen, sind dadurch häufig gut linderbar.
Die äußerlich erkennbaren Symptome sind nicht allein auf die Entzündung zurückzuführen, sondern auch durch eine ausgeprägte Schwellung des Nervengewebes um die Entzündung herum. Neben den entzündeten Nervenbahnen werden hierdurch auch umgebende Nervenbahnen in Mitleidenschaft gezogen. Cortison ist hier das Mittel der Wahl, weil es einerseits entzündungshemmend, andererseits aber auch abschwellend wirkt.
Ein Schub sollte stets ernst genommen werden. Er ist ein Notfall und ist so früh wie möglich zu behandeln, um den fortschreitenden Untergang von Nervenbahnen möglichst abzubremsen.
Wenn die Basistherapie erschöpft ist – die Eskalations-/Reservetherapie
Nach dem alten Stufenschema ist der Begriff Eskalationstherapie verankert. Hier muss es zukünftig eine Änderung geben. Neue Therapien (hier insbesondere Alemtuzumab) sind mit einem erheblichen Aufwand in der Anwendung und in der Überwachung der Maßnahme über Jahre verbunden. Nennen wir solche aufwändigen Therapien, die aber nicht nur für die Eskalation (d.H. als Second-Line Maßnahmen) zugelassen sind, deshalb Reservetherapie (bis ein besserer Begriff gefunden und eingeführt ist).
In der Eskalationstherapie oder besser in der Therapie der hoch aktiven Multiplen Sklerose werden aktuell Fingolimod (Gilenya®), Natalizumab (Tysabri®) und Mitoxantron (Ralenova®) angewendet. Als weiterhin sehr wirksames, aber auch in der primären Behandlung besonderes aktiver Formen der MS seit 2013 verfügbar ist Alemtuzumab.
Mitoxantron ist ein mittels Infusion verabreichtes Medikament, welches in höherer Dosierung auch in der Krebsbehandlung eingesetzt wird. Es schädigt sich vermehrende Immunzellen. Die Lebensendzeitdosis ist bei 100 mg/m2 Körperoberfläche erreicht (früher waren bis zu 140 mg/m2 Körperoberfläche zulässig). 12 mg/m2 Körperoberfläche werden in der Regel pro Behandlung (alle drei bis vier Monate) eingesetzt.
Eine mögliche Schädigung der Herzmuskelfunktion (Kardiotoxizität) ist möglich – vornehmlich bei höheren Dosierungen. Weiter sind bei dieser Behandlungsform Übelkeit, Unfruchtbarkeit und ein erhöhtes Krebsrisiko (Leukämie!) als Begleiterscheinung möglich.
Natalizumab wird im Einsatz in der Eskalationstherapie gegenüber Mitoxantron abgewogen. Es wird einmal im Monat gegeben und verhindert die Wanderung der fehlgesteuerten Immunzellen ins Gehirn und Rückenmark. Es hat seine hohe Wirkung (auf die Schubrate und die Kernspinaktivität) in zahlreichen Studien nachgewiesen. Diese Substanz hat den Begriff „frei von jeglicher Krankheitsaktivität“ geprägt, was bei über 30 % der Patienten erreicht wurde.
An Nebenwirkungen sind (überwiegend zu Beginn der Therapie) allergische Reaktionen möglich. Auch können im Zuge der Therapie die Infektanfälligkeit zunehmen und/oder Gelenkschmerzen (Arthralgien) auftreten. Leberschäden sind selten beschrieben, ebenso das Auftreten von Antikörpern, welche die Wirkung des Medikamentes beeinträchtigen. Die gefährlichste Komplikation im Rahmen dieser Therapie ist die so genannte progressive multifokale Leukencephalopathie (PML), eine sehr schwere Erkrankung des zentralen Nervensystems. Mit Stand Frühjahr 2013 ist es weltweit zu 347 Fällen bei über 112.000 behandelten Patienten gekommen; davon 123 in den USA, 203 aus der EU und 21 aus anderen Ländern. 20 % der betroffenen Patienten (79) sind an der PML verstorben
Die progressive multifokale Leukencephalopathie wird durch ein JC-Virus ausgelöst, welches nach dem Ersterkrankten John Cunnigham benannt wird. Es ist ein Virus, welches bei einer hohen Durchseuchung nach neueren Erkenntnissen bei ca. 50 bis 60 % aller mit einem speziellen Test untersuchten Menschen nachweisbar ist. Durch die Therapie oder auch durch eine immunsuppressive Therapie mit Zytostatika kann es ebenso wie bei immunschwachen Menschen (die an einem Tumorleiden oder an AIDS erkrankt sind) zu einer Vermehrung dieser Viren in Gehirn und Rückenmark kommen. Folge sind oft auffällige psychische Veränderungen, epileptische Anfälle, durchaus auch schubverdächtige Symptome. Besonderes solche Patienten, die JC Virus positiv sind und insbesondere solche, die vor der Natalizumabmedikation eine immunsuppressive Behandlung gegen ihre MS erhalten haben, sind gefährdet, eine PML zu erleiden.
Die PML ist ein Notfall, sie erzwingt den sofortigen maximalen diagnostischen Aufwand: eine Untersuchung der Rückenmarksflüssigkeit, eine stationäre Behandlung, die Kernspintomographie, das Absetzen der Medikation sowie eine besondere Form der Blutwäsche (Plasmapherese).
Nach der Zulassung von Fingolimod in den USA als orales(einmal täglich einzunehmendes) firstline Medikament in der MS-Therapie ist seit 2011 auch in Europa Fingolimod in der Therapie der MS einsetzbar. Allerdings ist es (vergleichbar der Zulassung von Natalizumab) nur für stark krankheitsaktive und in der Eskalationstherapie zugelassen. Fingolimod ist ein Medikament, welches die Wanderung von Immunzellen verhindert, indem es die fehlgesteuerten Immunzellen gewissermaßen in den Lymphknoten «einsperrt». Damit wird auch das Eindringen krankmachender Immunzellen (Lymphozyten) in das Nervensystem blockiert. Lymphknoten gehören zum Immunsystem des Körpers. Sie sind eine Art «Filterstation» für das Gewebewasser (Lymphe). Fingolimod hat seine Wirksamkeit in der Schubratenreduktion (über 3 Jahre ca 70 % der Patienten ohne Schub), und in der Verringerung neu auftretender, im Kernspintomograph sichtbarer Herde (nach 3 Jahren 87 % der Patienten ohne neue aktive Herde) bisher in vielen Studien und auch in der breiten klinischen Anwendung gezeigt. Eventuell hat Fingolimod eine weitere, sich im zentralen Nervensystem manifestierende neuroprotektive (d.h. schützende) Wirkung (66 bis 74 % der Patienten nach fünf Jahren ohne Behinderungsprogression).
Alemtuzumab ist seit 2001 bereits in der Behandlung bestimmter Formen der Leukämie zugelassen. Es ist ein monoklonaler Antikörper, der zwischenzeitlich auch bei der Multiplen Sklerose seine Wirkung bewiesen hat. Das Medikament wird als Infusion in einer Serie von fünf Infusionen innerhalb einer Woche im ersten Jahr und dann in einer Serie von zwei Infusionen im zweiten Jahr appliziert. Alemtuzumab ist nach ersten Studien in der Lage, die Rate der Schübe um etwa 74 % im Vergleich zu einer bereits zugelassenen hoch wirksamen Substanz (Interferon 1a in hoher Dosierung) zu verringern. Das Medikament beeinflusst autoreaktive T- und B-Lymphozyten.
Immunglobuline sind spezifische Eiweißbestandteile im Blutplasma. Sie werden aus Spenderplasma gewonnen und aufbereitet. Für Immunglobulintherapien bei MS gibt es keine generelle Zulassung, jedoch Genehmigungen im Einzelfall. In der Schwangerschaft und in der Stillzeit sind sie lange Jahre eingesetzt worden. Hauptproblem der Immunglobulingabe aus medizinischer Sicht ist die Möglichkeit allergischer Reaktionen, die bis zum Schock (z. B. bei IgA-Mangel-Patienten) führen können. Vor dem Hintergrund entsprechend vorsichtiger und aufwendiger Herstellungsverfahren kann inzwischen weitgehend ausgeschlossen werden, dass aus dem Blut der Spender Krankheitserreger übertragen werden.